- Телефон: +7 (495) 258-83-05
- E-mail: sales@electrochemistry.ru
Комплексонометрическое титрование

Титратор для комплексонометрического титрования. GT-310
Чтобы унифицировать получаемые результаты анализа и избежать индикаторной ошибки рекомендуется применять автоматизированные установки. Они позволят выполнять анализ в строго контролируемых одинаковых условиях, фотометрически детектируя смену окраса раствора.
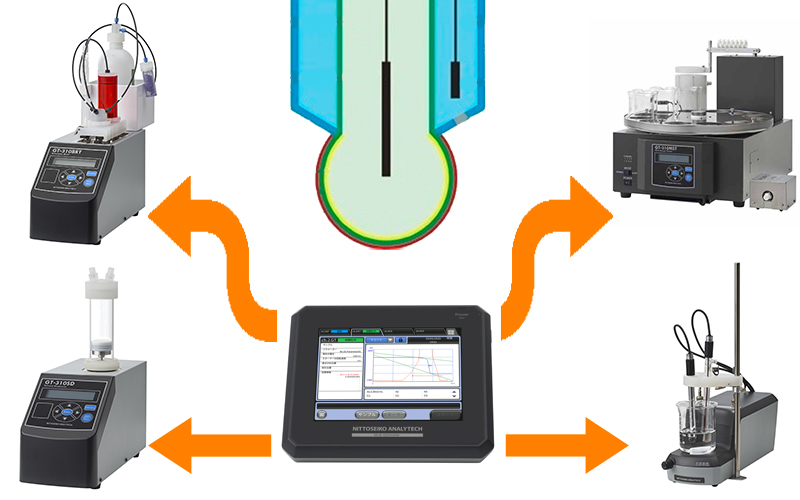
Комплектация автоматического лабораторного титратора для комплексонометрического титрования на примере модели GT-310 от японской компании "Mitsubishi Chemical Analytech Co., Ltd." (с 2020 года перешла в собственность «Nittoseiko Analytech»):
Основной блок – потенциометрический титратор GT-310 – управляется либо встроенным программным обеспечением, либо с помощью WINDOWS-совместимого ПО. Он производит все расчетные операции и сохраняет необходимые данные (концентрации, объемы, статистику и пр.) в памяти.
Бюретка для титрования GT-310BRT – предназначена для дозирования и титрования растворов. Можно задавать шаг, скорость, последовательность дозирования.
Фотометрический датчик GT-LDII – имеет встроенный детектор, вырабатывающий фототок при определенной длине волны. При смене окраса раствора длина волны меняется, изменяя фототок. В процессе подачи титранта объем поданного раствора можно зафиксировать до смены окраса индикатора и после.
Мешалка GT-310STR – позволяет производить контролируемое и повторяемое перемешивание пробы.
Это основные элементы автоматической системы для фотометрического титрования на базе потенциометрического титратора GT-310. Дополнительно к ним можно добавить устройства для автоматической подачи образцов, принтер для распечатки результатов, весы с возможностью передачи веса образца сразу в прибор и другие полезные модули.
Сущность комплексонометрического титрования
Комплексонометрическое титрование – это титриметрический метод анализа, основанный на взаимодействии определяемых ионов металла с комплексонами. Чаще всего в роли комплексообразователя выступает динатриевая соль этилендиаминтетрауксусной кислоты (другие названия: Трилон Б, ЭДТА), которая в большинстве случаев образует комплексы с катионами металлов в молярном соотношении 1:1, что упрощает расчет концентраций определяемых элементов.
Устойчивые комплексы с ЭДТА большинство металлов образуют в щелочной среде, для этого к раствору с анализируемым образцом добавляют аммиачный буфер, но некоторые элементы, например, железо (Fe III), можно титровать и в кислой среде.
Основные требования к комплексообразующему реагенту:
-
Образования устойчивых комплексов с катионами металлов в известном молярном соотношении.
-
Хорошая растворимость образуемых комплексов в воде.
-
Образующиеся комплексы не должны быть окрашены.
-
Взаимодействие комплексона с противоионом должно происходить быстро и количественно
Всем этим требованиям, в большинстве случаев, удовлетворяет Трилон Б.
Индикатор подбирают в зависимости от титруемого элемента и исходя из типа титрования.
Как уже упоминалось ранее, pH среды существенно влияет на устойчивость образующихся комплексов, что видно при построении кривой комплексонометрического титрования ионов кальция, представленной ниже:
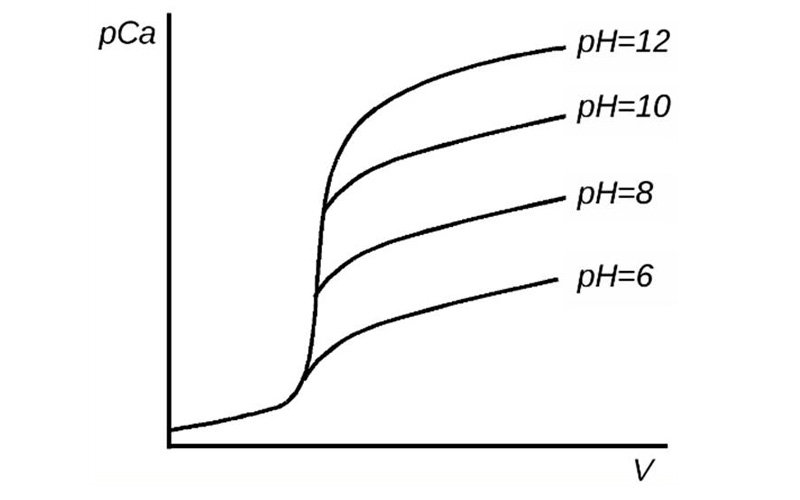
Рис.1 Кривая титрования [Ca2+] трилоном Б при различных значениях pH.
Из кривых титрования видно, что при более высоком pH величина ΔpCa больше (высокий скачок), что позволяет точней идентифицировать точку эквивалентности.
Классификация методов комплексонометрического титрования
Как и большинство титриметрических методов, комплексонометрию можно проводить прямым, обратным или заместительным титрованием.
-
В случае прямого титрования первоначальное окрашивание раствора вызвано взаимодействием индикатора с металлом. В дальнейшем сильный комплексообразователь трилон Б вытесняет индикатор, образуя с металлом более устойчивый комплекс. В ходе этого взаимодействия наблюдается смена цветности раствора. Титрант добавляется до получения устойчивого окраса, что говорит о присутствии в растворе свободного Трилона Б.
-
Обратный метод титрования подразумевает добавление избытка комплексона к раствору. Непрореагировавшую часть ЭДТА оттитровывают солью цинка или магния. Зная первоначально добавленный объем ЭДТА и вычтя из него количество оттитрованного избытка, можно вычислить содержание металла, вступившего во взаимодействие с комплексоном. Этот способ предпочтителен для элементов, которые медленно взаимодействуют с Трилоном Б, для которых сложно подобрать индикатор. Металлы в нерастворимых в воде солях тоже определяют обратным титрованием. Кроме того, если индикатор образует более прочный комплекс с металлом, чем титрант, то обратное комплексонометрическое титрование поможет определить его содержание.
-
При заместительном титровании к образцу добавляют комплексы металлов, которые легко вытесняются определяемыми металлами в образце. Избыток добавленного раствора оттитровывается стандартным раствором ЭДТА.
Комбинированные методы комплексонометрического титрования
Комбинацией упомянутых методов можно определять не только катионы, но и анионы, такие как SO42-; PO43-; CrO42-. Для этого их сначала осаждают, фильтруют, растворяют в известном количестве ЭДТА. Избыток ЭДТА оттитровывают сульфатом цинка.
Виды комплексонометрического титрования
Различают комплексонометрические методы в зависимости от используемого хелата:
-
Трилон Б – трилонометрия. Обычно применяется для определения катионов металлов.
-
Соединения ртути – меркуриметрия. Применяется для анализа анионов (галогенов, цианидов и пр.).
-
Фосфорорганические комплексоны. Применяются относительно недавно и позволяют специфично определять катионы металлов даже в смесях.
Можно классифицировать методы комплексонометрического титрования в зависимости от используемого индикатора.
Индикаторы для комплексонометрического титрования
Выбор индикатора в первую очередь зависит от условий титрования. Для анализа катионов металлов наиболее универсален индикатор Эриохром черный Т, который применяется для определения Mg+; Са2+; Zn2+; Cd2+; Pb2+; Мn2+.
Широкий спектр элементов можно определять с помощью Ксиленолового оранжевого, в том числе редкоземельные элементы, висмут и Fe3+.
Также в комплексонометрическом титровании используют такие индикаторы, как: Пирокатехиновый фиолетовый, Мурексид, кальцес, Хромовый темно¬синий, Бериллон II, Кальцион, Кальцеин и пр.
При индикаторном титровании необходимо четко фиксировать смену окраса индикатора для определения конечной точки титрования. Учитывая особенности индивидуального цветовосприятия, момент перехода окраса у разных лаборантов может отличаться, что влияет на точность получаемых результатов, повторяемость.
Применение комплексонометрического титрования
Методы комплексонометрического титрования особенно важны при определении Ca и Mg при анализе воды на жесткость (ГОСТ 52407-2005, ГОСТ 4151-72, ПНД Ф 14.1:2.98-97 и др. методики). Эти показатели определяют ее целевое назначение и пригодность для бытового и технологического использования. Кроме этого существуют внутренние нормативные документы на предприятиях, которые регулируют качество используемой воды и методы ее анализа.
Методики определения других элементов востребованы в различных отраслях химической промышленности. Эти задачи решаются титрованием. В ГОСТ 10398-2016 представлены методы анализа для широкого перечня элементов в составе реактивов и особо чистых веществ.