- Телефон: +7 (495) 258-83-05
- E-mail: sales@electrochemistry.ru
Кислотно-основное титрование

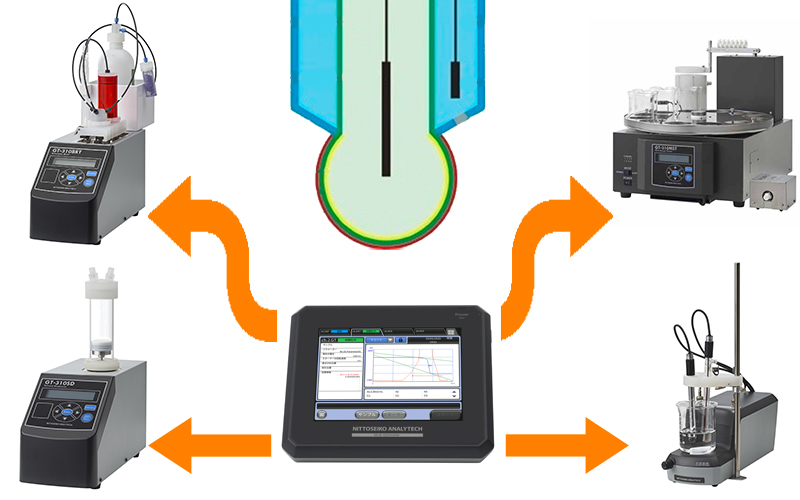
Титратор для кислотно-основного титрования. GT-310
Автоматизация методик анализа повышает точность измерения, повторяемость и воспроизводимость результатов. Настроив нужный метод один раз, можно не беспокоиться о влиянии человеческого фактора на результат измерения. Это особенно полезно для предприятий, практикующих вахтовый метод, когда доступ к одной установке имеют несколько сотрудников.
Стандартный комплект для потенциометрического титрования на базе прибора GT-3100 (совместная разработка "Mitsubishi Chemical Analytech Co., Ltd." и "Nittoseiko Analytech", Япония) включает:
-
базовый блок для титрования (автоматический титратор);
-
бюретку, с помощью которой контролируется объем подаваемого раствора;
-
магнитную мешалку с контролем перемешивания;
-
систему электродов для кислотно-основного титрования.
Подходящие электроды для потенциометрического титратора GT-310
Выбор электродов зависит от растворимости аналита в воде.
Для водного титрования рекомендован комплект, состоящий из раздельной пары электродов.
Эта же система электродов, помещенная в общий корпус, называется комбинированным электродом. Компания «Mitsubishi Chemical Analytech» предлагает два варианта исполнения комбинированных электродов для титрования водных сред:
Кислотно-основное титрование неводных сред особенно удобно выполнять на автоматическом приборе, поскольку это избавляет лаборанта от контакта с уксусной кислотой, используемой для анализа.
Система для неводного титрования включает:
• измерительный стеклянный pH-электрод GTPH1B;
• электрод сравнения для водных и неводных сред GTRS10B.
Именно такой комплект описан в ГОСТ 11362-96 (определение числа нейтрализации в маслах и нефтепродуктах).
Дополнительно прибор можно оснастить весами с автоматической передачей веса образца в прибор, принтером и дополнительными разъемами для подключения датчиков другого типа.
Сущность кислотно-основного титрования
Кислотно-основное титрование – это метод объемного титриметрического анализа, основанный на реакции нейтрализации, позволяющий определять концентрации кислот или оснований в водных и неводных средах.
Суть кислотно-основного титрования сводится к передаче протона либо от титранта к аналиту, либо, наоборот, от аналита к титранту. В процессе анализа необходимо точно определить, когда количество добавленного компонента будет ЭКВИВАЛЕНТНО количеству измеряемого компонента. Этот момент называют ТОЧКОЙ ЭКВИВАЛЕНТНОСТИ (ТЭ). В случае КО титрования точка эквивалентности будет достигаться при строго определенном значении pH, поэтому для ее определения используют индикаторы. По мере добавления кислоты/основания, сразу после прохождения ТЭ, в растворе будут появляться/исчезать свободные протоны и индикатор поменяет окрас раствора. Также изменение pH среды можно отслеживать потенциометрически. В этом случае регистрируют скачок потенциала при достижении ТЭ.
При определении содержания кислот в качестве титранта используют растворы KOH, NaOH или Ba(OH)2 известной концентрации. Определение концентрации оснований проводится растворами сильных кислот: HCl или H2SO4.
Перед началом анализа необходимо определить точную концентрацию титранта.
Щелочи стандартизируют гидрофталатом калия.
Другой способ приготовления титранта с точно известной концентрацией – использовать фиксанал.
При работе с щелочами нельзя допускать их контакта с воздухом, поскольку содержащаяся в нем углекислота легко поглощается титрантом, из-за чего меняется его концентрация. Хранить щелочи в стекле долгое время тоже нельзя, поскольку они с ним взаимодействуют.
Кривые кислотно-основного титрования
Кривая КО титрования строится в координатах: pH раствора – объем добавленного титранта.
На кривой обычно видны две точки перегиба (ТП), между которыми находится точка эквивалентности.
Расстояние ΔpH между точками перегиба называется скачком титрования. Его величина зависит от концентраций реагентов. Чем выше концентрация титранта, тем больше скачок, вызванный сменой кислотности раствора в районе ТЭ. Этот скачок вызывает резкую смену окраса индикатора.
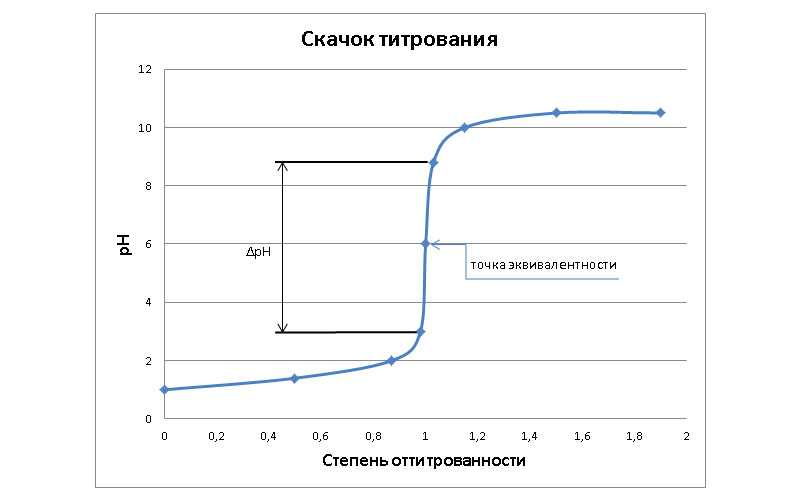
Вид кривых кислотно-основного титрования будет зависеть от природы реагирующей пары: кислота-основание.
Можно рассмотреть следующую классификацию кривых титрования:
-
сильная кислота – сильное основание
-
слабая кислота – сильное основание
-
сильная кислота – слабое основание
-
слабая кислота – слабое основание
Все они будут отличаться величиной скачка титрования и областью расположения точки эквивалентности.
При титровании многоосновных кислот их диссоциация происходит ступенчато, поэтому на кривой титрования будет несколько точек перегиба. ТП могут попадать в разные диапазоны pH, в таких случаях для их идентификации требуются индикаторы с различным рабочим интервалом.
Смеси кислот (оснований) будут охарактеризованы еще более сложными кривыми. На них возможны наложения точек перегиба, что затрудняет точную идентификацию ТЭ ручным способом анализа.
Индикаторы для кислотно-основного титрования
Все индикаторы работают в определенном интервале pH, который должен попадать, хотя бы частично, в диапазон скачка титрования.
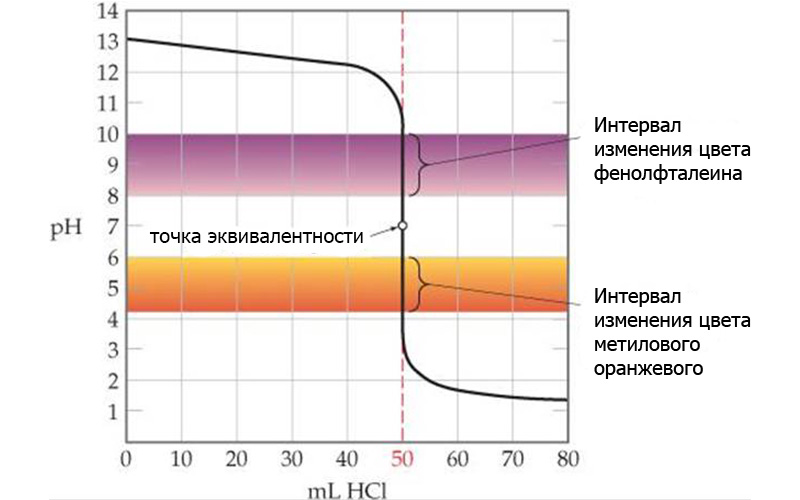
Например, фенолфталеин меняет окрас в диапазоне pH=8-10, в то время как смена цвета метил оранжевого происходит при pH=4-6. Это значит, что индикаторы реагируют не на достижение точки эквивалентности, а именно на pH-раствора – и это нужно учитывать при подборе индикатора.
Именно поэтому электрохимические методы анализа являются более универсальными. Потенциометрический титратор построит полную кривую титрования и автоматически рассчитает точку эквивалентности по скачку потенциала.
Применение кислотно-основного титрования
Потенциометрический метод кислотно-основного титрования получил широкое распространение для определения кислотных и щелочных чисел в нефтепродуктах. В Фармакопее также представлены методы неводного КО титрования. В химической промышленности для контроля концентраций кислот и щелочей применяется анализ в водных средах.